שיטות מוקדמות לאבחנה טרום לידתית
מחבר: ד"ר אייבי לוין
מתוך: הכינוס השנתי הראשון לרבנים ורופאים בנושא: גניקולוגיה, פוריות ויילודים לאור ההלכה
פסח תשנ"ב - אפריל 1992
תקציר: המאמר מתאר את השיטות השונות לאבחון מצבו של העובר טרם לידתו.
מילות מפתח: מומים מולדים, אולטרה-סאונד, תסמונת דאון, אבחון גנטי, די.אנ.אי, דיקור מי שפיר, סיסי שליה, חלבון עוברי.

מומים מולדים, תכופות על רקע גנטי, מאיימים על חייהם ויכולת תפקודם של שלושה מכל מאה יילודים. מומים אלה מהווים 20% מסיבות המוות של יילודים, ושיעור גבוה עוד יותר של הסיבות לתחלואה קשה בגיל הילדות.
עלות הטיפול והשיקום בילדים אלו היא עצומה, והסבל הנגרם לילדים ולמשפחותיהם אינו ניתן כלל להערכה. מצד שני, היכולת לאבחן מומים גנטיים עוד במהלך ההריון השתפרה באופן ניכר בשני העשורים האחרונים, בעיקר עקב שיפורים טכניים בשטח הביולוגיה המולקולרית והאולטרה-סאונד, שאיפשרו הקדמת האיבחון הטרום לידתי מהשליש השני של ההריון - לשליש הראשון שלו. לרשותנו עומדות היום מגוון של טכניקות, והאיבחון הטרום-לידתי יכול להתבצע בדם העובר, בתאים עובריים במי השפיר, ובסיסי השליה. זיהוי אותם הריונות הנמצאים בסיכון מוגבר כרוך באיתור גורמי סיכון ע"י שיטות סריקה לא-חודרניות, כמו בדיקת דם לאישה ההרה, ובדיקה בעזרת מכשיר אולטרה-סאונד.
בדיקת דם לאישה ההרה
השיטה הקלה ונפוצה ביותר היא בדיקת דם לאישה ההרה, סביב לשבוע ה-17 להריון, שהוא תחילת החודש החמישי, ובה נמדדים רמת החלבון העוברי, רמת ההורמון השלייתי ורמת ההורמון אסטריול בדם האם. החלבון העוברי בו מדובר כאן הוא חלבון שמקורו בעיקר בכבד העובר, הוא מופרש ברובו למי-השפיר, ועובר בכמויות קטנות דרך הרחם לדם האם. עצם נוכחות החלבון בדם האם אינו מפריע לאם או להריון, אך במקרים של מומים פתוחים במערכת העצבים של העובר נמצא רמות גבוהות במי השפיר, ובעקבות זאת גם בדם האם. בדיקת דם פשוטה הנלקחת מהאם עשויה לגלות לנו מהי רמת החלבון העוברי בדם האם, ולסייע לנו להעריך מהו הסיכוי שאישה זו נושאת עובר בעל מום הקשור למערכת העצבים המרכזית, או מום בדופן הבטן. היישום השגרתי של אמצעים אלה העלה את שכיחות הגילוי של פגמים פתוחים במערכת העצבים המרכזית, כמו ספינה ביפידה פתוחה והתפתחות לא תקינה של המוח (אננצפלוס), ומומים בדופן הבטן של העובר כמו גסטרוסקיזיס ואומפלוצלה. גם רמה נמוכה מן התקין של החלבון העוברי ושל האסטריול בדם האם מסמנים סיכון מוגבר למומים כרומוזומליים, כמו טריזומיה 18 וטריזומיה 21.
הבעיה העיקרית ביישום האיבחוני של הבדיקה היא, שכמו בכל תופעה ביולוגית גם כאן התפלגות הערכים נמצאת בטווח רחב, עם חפיפה בשוליים בין העובר הנורמלי לבין העובר הפגום. סקר האוכלוסיה לרמות חלבון עוברי בדם האם לגילוי מומים במערכת העצבים מכסה לכן רק 98% מההריונות הנורמליים, ו-2% מההריונות האלה יכנס לתחום שמעל 2.5 MOM, שנקבע כגבול העליון של הנורמה. כלומר, אם בעשרת אלפים הריונות ישנם כרגיל עשרה מקרים של מום פתוח במערכת העצבים, הרי שלושה מההריונת האלו לא יתגלו ע"י הסקר המקדים הזה, ועשויים להתגלות רק ע"י בדיקה בעזרת אולטרה-סאונד שיאבחן את הפגם המסויים הזה במערכת העצבים. לעומת זאת, למרות שהערך של 2.5 MOM ויותר נחשב לערך גבוה, וקשור בשכיחות גבוהה לאותם מומים שהזכרתי, קיימים מצבים שאינם קשורים למומים האלו שגם בהם קיימת רמה גבוהה של החלבון בדם האם יחסית לשבוע ההריון בו האישה נמצאת, כמו למשל הריון מרובה עוברים, הריון מתקדם יותר מאשר גיל ההריון המשוער, מוות תוך-רחמי של העובר ופיגור בגדילה התוך-רחמית. כמו-כן יש לקחת בחשבון בפרשנות של הנתונים גם את משקל האישה, ואת האפשרות שיש לה סכרת.
אולטרה-סאונד ודיקור מי שפיר
המצבים שהוזכרו לעיל, כמו גם רוב מקרי המומים המולדים שהוזכרו, ניתנים לאיבחון בעזרת האולטרה-סאונד, ולכן בכל מקרה בו נמצא ערך מוגבר בדם האישה היא מופנית לבדיקת אולטרה-סאונד. במידה והבדיקה אינה מעלה ממצא חריג - מומלץ לאישה לבצע דיקור מי שפיר. בכל מקרה בדיקת הדם חייבת להתבצע לפני דיקור מי השפיר, כיוון שהדיקור מעלה את רמת החלבון העוברי בדם האם. מטרת דיקור מי השפיר היא לברר ולקבוע מהי רמת החלבון העוברי במי השפיר עצמם, כי ישנם מקרים בהם רמת החלבון העוברי גבוהה בדם האם אך תקינה במי השפיר, מסיבות שאינן קשורות לאותם מומים שאנו מחפשים. באותו הקשר בודקים גם את רמת האצטיל-כולין-אסטראז, שגם הוא רמתו במי השפיר מוגברת רק במומים פתוחים של מערכת העצבים, וגם את הקריוטיפ (המטען הכרומוזומלי של העובר), כדי לוודא את תקינותו.
בדיקת רמת החלבון העוברי לגילוי תסמונת דאון
השימוש בבדיקת רמת החלבון העוברי בדם לגילוי טריזומיה 21 (תסמונת דאון) היא הרבה פחות ספציפית, מאשר השימוש בה לגילוי מומים פתוחים של מערכת העצבים, עקב החפיפה הגדולה-יותר בתוצאות הבדיקה עם ההריונות הנורמליים; לכן משלבים בסקירה גם את רמת הגונדוטרופין הכוריוני HCG. הורמון זה מופרש ע"י השליה, והערך הגבולי העליון שלו משתנה לפי גיל האישה. גם כאן, אם נמצא ערך מוגבר, נפנה את האישה לבדיקת אולטרה-סאונד, עקב האפשרות של טעות בגיל ההריון וכד', וכן עקב שינויים פתולוגיים בשיליה, שגם הם יכולים לגרום להפרשה מוגברת של ההורמון הזה. גם ערך נמוך של HCG הוא משמעותי - לעומת הערך הגבוה הקשור יותר לטריזומיה 21 (תסמונת דאון), הערך הנמוך יותר קשור למום כרומוזומלי אחר - טריזומיה 18, שהוא פגם חמור מאוד בפני עצמו.
ברמות אסטריול נמוכות עולה הסיכון לטריזומיה 18, איכטיוזיס בתאחיזה לכרומוזום X, היפרפלאזיה של יותרת הכליה והפלות נדחות, כל אלה מחלות שניתן לאבחן אותן באמצעים נוספים. הסקירה הזאת נותנת רק אינדיקציה לגבי סיכוי מוגבר לנוכחות של אותו פגם, בשום אופן לא אבחנה סופית. זה נכון לגבי כל המדדים שאמרנו קודם, גם לגבי החלבון העוברי, גם לגבי ה-HCG וגם לגבי האסטיול. אולם ניתן לומר, שבשילוב שלושת הסמנים האלו בדם האם עם סקירה לאיתור מומים בעזרת האולטרה-סאונד, ניתן להגיע לגילוי מוקדם של 70% מהמומים העובריים. זה הישג שבהחלט פותח צוהר לעתיד טוב יותר בנושא הזה של האיבחון. כמובן שכל החלטה אם לבצע בדיקות חודרניות להמשך הבירור חייבת להסתמך על ייעוץ גנטי, הנעזר במידע על העבר הרפואי של האישה והבעל, בעיקר אם מישהו במשפחתם הקרובה סבל ממום מולד או מחלות תורשתיות, בדיקת אפשרות של חשיפה לתרופות או זיהומים העלולים לפגוע בעובר, וכן הריונות קודמים של האישה ומידת תקינותם - מפני שלידת תינוק אחד בעל תיסמונת דאון מעלה את הסיכוי ללידת יילוד נוסף בעל תסמונת כזו ל-1:100, וכן מום במערכת העצבים אצל תינוק אחד מכפיל את הסיכון פי עשרים ללידת תינוק נוסף כזה.
דיקור מי שפיר
הטכניקה של דיקור מי שפיר תוארה לראשונה בשנת 1952, והוכנסה לשימוש קליני לאיבחון הקריוטיפ של העובר (המטען הכרומוזומלי שלו) ב-1966. הטכניקה היא כזו: דופן הרחם נדקר דרך דופן הבטן באמצעות מחט דקה ובהנחיית אולטרה-סאונד, כמות מסויימת של מי שפיר נשאבת, והתאים שנשרו מהעובר מסוננים מתוכם ומודגרים בתרבית עד לחלוקתם, ואז נבדק מבנה הכרומוזומים שלהם. משך הזמן הדרוש לקבלת תשובה מותנה במהירות צמיחת התאים בתרבית, ונע בין עשר לעשרים יום. לעתים קורה שהתאים אינם גדלים בתרבית, או שמתקבלת תשובה לא-ברורה, כמו מוזאיקה [ז"א שבאחת מצלחות גידול התרבית צמחו תאים לא תקינים, וביתר הצלחות - תאים תקינים], ואז נזקקים לשיטת איבחון חלופית, כמו דגימת דם העובר.
מאז הכנסתה לשימוש שיגרתי משמשת שיטת דיקור מי השפיר כסטנדרט שמולו נבחנות כל השיטות האחרות לאיבחון טרום-לידתי, הן מבחינת יעילותן האיבחונית והן מבחינת הסיכונים, כאשר הסיכון העיקרי הוא איבוד ההריון כתוצאה מהפעולה, סיכון שמוערך בחצי אחוז עד אחוז אחד. אבל ישנם גם סיבוכים נוספים מדיקור מי השפיר, שיש לקחתם בחשבון. ביילודים שנדקר שק מי השפיר שלהם נמצא שיעור גבוה יותר של מצוקה נשימתית ודלקת ריאות, שכיחות גבוהה יותר של הפרעות אורטופדיות ועליה בשכיחות מעבר כדוריות דם אדומות מהעובר לאם כתוצאה מהדיקור.
גישה ישירה למחזור הדם העוברי
גישה ישירה למחזור הדם העוברי לצרכי איבחון וריפוי הייתה משאת נפשם של רופאי היילודים, מאז ומתמיד. דגימת הדם העוברי הראשונה נעשתה ב-1964 בפתיחת הרחם כדי להגיע אל חבל הטבור ולקחת ממנו דגימת דם. רק ב-1974 תוארה טכניקה של הכנסת פטוסקופ, מכשיר אופטי, אל תוך חלל הרחם, לנטילת דגימה של דם העובר באמצעות דיקור חבל הטבור במחט. גישה זאת איפשרה התקדמות נרחבת בהבנתנו את הפיסיולוגיה של עובר האדם, ועומדת בבסיס האיבחון והנחיית הטיפול המיילדותי במחלות העובר. השימוש הנפוץ ביותר הוא בטיפול במחלות הדם של העובר הגורמות לאנמיה. מחלות אלו כוללות בחלקן הפרעה במבנה ההמוגלובין בכדוריות הדם האדומות (ההמוגלובין אחראי לנשיאת החמצן בכדוריות הדם האדומות) כמו מחלת הטלסמיה. פגם זה ניתן לאיבחון במי השפיר, אך גם בסיסי השליה ובדם העובר, והבחירה תתבסס על זמינות הטכניקה והמעבדה ועל גיל ההריון. לעומת זאת, במחלות בהן האיבחון תלוי בקבלת מידע הקשור למספר ופעילות הכדוריות האדומות, הכדוריות הלבנות והטסיות, האיבחון יוכל להיעשות רק באמצעות דגימת דם ישירה של דם עובר מחבל הטבור.
באותה טכנולוגיה של חדירה לכלי דם של העובר ניתן גם לטפל באותם סיבוכי הריון, כמו למשל עירוי דם תוך רחמי לעובר, לאבחן מומים מולדים ולאבחן הריון עם פיגור בגדילה. יתרון חשוב נוסף של דגימת הדם היא היכולת הבלעדית לאבחן, אצל אישה שחלתה בזיהום תוך-רחמי, אם העובר נפגע ממחלות זיהומיות. רשימת הזיהומים כוללת טוקסופלזמוזיס, אדמת, ציטומגלווירוס CMU, אבעבועות, פרבווירוס ואיידס. לא כל הזיהומים האלה גורמים לנזק לעובר, ישנם הרבה מקרים שהאם חלתה והעובר לא נפגע. עובר לא יכול להיפגע מהמחלות האלה אלא אם כן הווירוס חדר אל העובר עצמו, ובחלק גדול מהמקרים הוירוס לא חודר אל העובר. ניתן לאבחן את אותם מקרים שהוירוס חדר לעובר ע"י בדיקת תגובת מערכת החיסון של העובר, וליתר דיוק את הופעת האימונוגלובולינים מסוג IgM. עם המידע הזה אפשר לשקול מה עושים לגבי אותו הריון, במידה שקיימת ודאות שאותו הריון אמנם נפגע ע"י הוירוס. אפשר לעומת זאת לעבור בשקט יחסי את אותו הריון בו לא נמצאה הוכחה של זיהום, ואנחנו יודעים שהעובר לא נפגע. שיעור איבוד ההריון כתוצאה מדגימת הדם העוברי המבוצעת בדרך כלל מחבל הטבור הוא כ-1%.
ביופסיות מעור העובר
גישה אבחנתית נוספת לאיבחון בעיות בעובר היא ביופסיות מעור העובר, שנעשות במגוון של מחלות עור קשות, כמו אפידרמוליזיס בולוזה, איכטיוזיס ואלביניזם. אנחנו מבצעים החדרה של מלקחיים מאוד עדינות דרך מחט לתוך חלל האם, ובהנחיית אולטרה-סאונד נלקחת פיסת עור קטנה מאוד מהעובר, בסדר גודל של בערך מילימטר. ניתן מפיסת העור הקטנה הזאת לאבחן את המחלות הקשות האלה בעוד העובר ברחם.
דגימת סיסי השליה
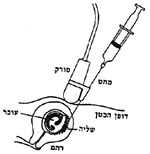
שיטת 'דגימת סיסי השליה' היא טכניקה חדשה שהוכנסה בשנים האחרונות כחלופה מוקדמת (בשליש הראשון של ההריון) לדיקור מי השפיר, מאחר ודיקור מי השפיר במתכונתו המסורתית נעשה בשליש השני של ההריון. טכניקת דגימת סיסי השליה הוכנסה לשימוש עקב יכולתה לאיבחון גנטי בשליש הראשון של ההריון, עם אפשרות לתשובה תוך ימים ספורים, במקום עשר עד עשרים יום הדרושים לתרבית תאים בשיטת מי השפיר. בדגימה של סיסי השליה מוחדר צנטר דרך צוואר הרחם או מחט דרך דופן הבטן, בהנחיית אולטרה-סאונד, ונשאבים סיסים מאיזור השליה [ראה תרשים]. כמות התאים המתקבלת גדולה מזו שבבדיקת מי השפיר, וניתן לעשות בה מגוון רחב מאוד של אבחנות טרום-לידתיות, בייחוד באיבחון מחלות אנזימטיות או ע"י אנליזה של DNA. נוסף לכך מתקצרת באופן משמעותי תקופת החרדה שהזוג נמצא בה עד לקבלת התשובה. לא פחות חשוב הוא ישום טכניקות חדשות שלא ניתן היה לבצען בבדיקת מי השפיר, המאפשרות איבחון מדויק יותר של פגמים גנטיים, ביוכימיים והמטולוגיים בשליש הראשון, פגמים שבעבר נזקקנו לדגימת דם מהעובר לצורך האיבחון שלהם. הבדיקה הזאת מתבצעת בדרך כלל בסביבות השבוע העשירי עד ה12- של ההריון, אם כי במקרים מיוחדים אנחנו מבצעים אותה בשבוע השביעי של ההריון, כך שניתן לקבל תשובה לגבי מצב העובר, אם הוא חולה או לא, כבר לפני היום הארבעים מההתעברות. בצענו את הפרוצדורה הזאת במספר מקרים שהייתה הנחייה הלכתית לבצע את הבדיקה לפני היום ה-40 של ההתעברות. כמובן שאצל הנשים אצלן הדבר נעשה היה סיפור משפחתי קודם של מומים תורשתיים קשים מאוד. בכל אותם מקרים נתנו תשובה לפני היום ה-40.
המגבלה הנגזרת מלחץ הזמן היא שאמינות התשובה המהירה (תוך 2-4 ימים) היא רק של 98%. תשובה סופית ניתן לקבל רק מתרביות תאים אחרי עשרה ימים עד שבועיים, וגם בהם דרגת הדיוק נופלת מעט מזו של בדיקת מי השפיר. יכולה גם לקרות טעות באיבחון, עקב ההבדל במקור התאים בין השליה והעובר.
בעובר בגיל שבין 4-8 ימים ישנה דיפרנציאציה של מסת התאים הפנימית, בנפרד ממסת התאים החיצונית. אחרי הדיפרנציאציה הזאת מסת התאים הפנימית תתפתח לעובר, והחיצונית לשליה וקרומים. שינויים בכרומוזומים שעשויים לקרות אחרי שלב זה יכולים להביא למצב שבדגימת סיסי השליה יכול להימצא מום כרומוזומלי שלא ימצא אצל העובר. לאחרונה תואר מקרה של טריזומיה 9 שנמצאה אך ורק בשליה, והעובר היה בריא לחלוטין. במקרים אחרים יכולה להתקבל מוזאיקה, כאשר חלק מהתאים תקינים וחלק מצביעים על עובר פגום. דבר זה קורה בערך באחוז אחד מהמקרים בהם ניטלו דגימות סיסי השליה. סיבה נוספת לטעות באיבחון היא חדירה של תאים אמהיים, שעלולים להישאב לתוך מחט השאיבה בעת המעבר דרך הרחם. גם בדיקור מי השפיר יכולה להיות אי התאמה. גם כאן המקורות השונים של התאים, כמו רקמות העובר, הקרומים ותאים אמהיים עלולים ליצור אי התאמה בין תוצאות הבדיקה לבין מצבו האמיתי של העובר. מוטציות בכרומוזומים עלולות לנבוע מהתרבית עצמה, כלומר מהתנאים בהם נמצאת התרבית עלולים להתפתח שינויים בכרומוזומים. אבל אי-ההתאמה הזאת היא נדירה, ובסיכום של למעלה מ-100,000 מקרים של דיקורי מי שפיר בשליש השני נמצאה שכיחות של מוטציות כזאת בתחום שבין 0.1-0.3 אחוז.
תוצאות דגימת סיסי השליה של יותר מ-60,000 מקרים המדווחים בספרות מראה שכיחות של מומים כרומוזומליים פי 1.5 מאשר בדגימת מי השפיר, וזה גם מובן, כי הבדיקה נעשית בשלב מוקדם יותר של ההריון, ומגלים מומים שבהמשך היו גורמים להפלה עצמונית ולא היו מגיעים כלל למועד של בדיקת מי השפיר. אחוז גילוי המומים לשבועות השונים אינו שונה משמעותית מדגימת מי השפיר, וב-98% מהמקרים מושגת דגימה מספקת לאיבחון עם כשלון מעבדתי קטן מאוד, פחות מאחוז אחד. שיעור איבוד ההריונות הוא כ-3-4 אחוז. המספר הזה נראה גדול, בהשוואה לחצי אחוז עד אחוז במי שפיר, או עד 1% בדגימת דם; אך אין לשכוח שהוא כולל בתוכו גם את אותן ההפלות שהיו קורות באופן טבעי ועצמוני בלי קשר לבדיקה הזאת, בגיל הצעיר של ההריון שעליו אנחנו מדברים, והסיכון המחושב שנוסף לפעולה עצמה הוא רק אחוז או שניים (סיכון של 0.6-0.8 אחוז מעבר לסיכון בדיקור מי שפיר, הפרוצדורה המסוכנת מעט יותר).
יש להזכיר נושא נוסף שעלה לאחרונה, והוא שכיחות מוגברת של מומי גפיים שתוארה לאחר דגימת סיסי שיליה. הפגמים התבטאו בעיקר במומים באצבעות. הסיבה לכך אינה ידועה, ויתכן שהיא על רקע של בעיה באספקת דם. התופעה אינה שכיחה, והיא תוארה רק ב-1:250-1500 מקרים, רובם בגיל הריון צעיר מ-66 יום. תוארו גם מקרים של מיעוט קיצוני של מי שפיר כתוצאה מהבדיקה.
דיקור בהנחיית אולטרא-סאונד
בשנים האחרונות, עם השיפור ביכולת ההדמיה, ניתן היה להיכנס לתחום של דיקור מי שפיר בשליש הראשון של ההריון. הנושא הזה בא לגשר בעצם בין יכולת האיבחון המוקדמת של דגימת סיסי השליה בשליש הראשון של ההריון, לבין דרגת האמינות של דיקור מי השפיר בשליש השני. עדיין נשאלות מספר שאלות ביחס לאמינות ובטיחות השיטה. הדיקור נעשה תחת הנחייה של מכשיר אולטרה-סאונד, בדומה לדיקור מי השפיר בשליש השני. אבל ישנה בעיה, מאחר וגודל השק הרבה יותר קטן מאשר בשליש השני של ההריון, ואנחנו מוגבלים בכמות המינימלית של הנוזל שניתן לשאוב, כי למעבדה יש את הצרכים שלה, לכן באופן יחסי כמות הנוזל שנשאב גדולה יותר ביחס לנפח הכולל של מי השפיר, מאשר הכמות הנשאבת בשליש השני של ההריון. ולכן נשאלו מספר שאלות: האם ניתן לקבל בקלות מי שפיר מתוך שק האמניון בשבוע כל כך מוקדם? התשובה לכך היא חיובית. האם ניתן לקבל מספיק תאים לאיבחון בהריון כה צעיר? והתשובה גם לכך חיובית, והתוצאות היום דומות מאוד לאלה של דגימת סיסי השליה. וישנן שאלות נוספות: האם דיקור שק האמניון בשבוע מוקדם לא יעלה את מספר איבודי ההריון? האם ריקון, ולו לתקופה מוגבלת, של נפח ניכר ממי שפיר, אינו עלול להעלות את שכיחות הבעיות האורטופדיות והנשימתיות ביחס לדיקור מי שפיר רגיל? מה שכיחות העירוי בין עובר לאם? מה שכיחות הפגיעה המכנית בעובר הצעיר בעקבות הפעולה, ומהי חומרתה? לכל אלה אין עדיין תשובות חד-משמעיות.
אנליזה של DNA
כמה מלים על טכניקות האיבחון. אנליזה של DNA: בשיטה זו אין צורך בתאים בחלוקה, אלא כל תא מגורען, בכל שלב של דיפרנציאציה, יכול לשמש לאיבחון. הטכניקה משמשת לאיבחון מחלות, כמו ציסטיק פיברוזיס, דושן והמופיליה, אשר לגביהן בהיעדר סיפור משפחתי אין אפשרות לסקר של נשים. השיטה כוללת איבחון ישיר ואיבחון עקיף. את האיבחון הישיר ניתן לבצע למוטציות ידועות שיש עבורן גלאי ספציפי לאותה מוטציה. לאחרונה הוחל בישום שיטה PCR, בה ניתן לשכפל במספר שעות מליוני העתקים של איזור DNA מסוים, שחלק מהמבנה שלו ידוע, ויתאפשר בכך להגדיל את מגוון האבחונים. האיבחון העקיף מתבצע בשיטה של אנזימי רסטריקציה בהם רצף DNA שונה עשוי להיות מזוהה ע"י גלאי מסומן, לאחר עיכול שרשראות DNA ע"י חלבון מעכל.
איבחון תאים עובריים בדם האם
נושא חדש ביותר הוא איבחון תאים עובריים בדם האם. כלומר, למעשה מה שהאיבחון הטרום-לידתי חותר אליו היום הוא להחליף את הבדיקות החודרניות שתוארו כאן בדגימת דם מהאם, וממנה להשיג תאים עובריים, מפני שיש מעבר של תאים עובריים דרך השליה לדם האם בכל הריון. בשיטה חדשנית זאת מבוצעת הפרדת תאים מדגימת דם שנלקחת מהאם ע"י מערכת לייזר, היכולה למדוד את גודל התאים, סדירות שטח הפנים או הימצאות נוגדנים מסומנים על גבי התאים. בשיטה אחרת מצמידים גלאים מגנטיים לאנטיגנים על פני התא, המאפשרים הוצאת התאים מהתמיסה. קיימות גם טכניקות, כפי שהזכרנו קודם, של אנליזה של תאים בודדים וטכניקה של היברידיזציה, וניתן היום ברמה של תאים בודדים להגיע לאבחנות. כמובן שזה עדיין לא בשימוש שוטף, מדובר עדיין בפרויקט מחקרי בשלבים ראשוניים, אך הוא בעל עתיד גדול.
איבחון הגנטי בשלב שלפני ההשרשה
נושא שנכנסנו אליו לאחרונה הוא האיבחון הגנטי ברמת התא, בשלב שלפני ההשרשה. במשפחות שבהן יש מחלות תורשתיות קשות, ניתן בשיטות של ביופסיה של תא בשלב של עובר בין 4-8 תאים לקחת דגימה או ביופסיה מהעובר. ע"י השיטה של אמפליפיקציה של DNA ניתן להגיע לישום אבחנתי בקביעת המין, במחלות כמו ציסטיק פיברוזיס, דושן, לש-ניאן וטלסמיה. האיבחון המוקדם של הפרעות תורשתיות עשוי לאפשר התערבויות טיפוליות מוקדמות במועד בו יש סיכוי לתוצאות חיוביות. למשל טיפול תרופתי מוקדם כמו בהיפרפלזיה של יותרת הכליה, או השתלת מח עצם במחלות בהן ניתן יהיה אולי להביא לריפוי חלקי או מלא של המחלה. ההשתלה חייבת להתבצע בגיל הריון צעיר יחסית, מאחר והנסיון בעולם מראה שהשתלה מאוחרת רבים סיכוייה להידחות. הנסיון שקיים היום בעולם לגבי השתלת מוח עצם לעוברים מצומצם מאוד. אנחנו עשינו זאת מספר מקרים במחלות קשות ביותר, אבל נכון להיום התוצאות אינן טובות, אולי בגלל גיל ההריון היחסית מתקדם בזמן ביצוע הטיפולים, ויתכן שהקדמת גיל ההריון בעתיד תיתן סיכוי טוב יותר לשיטה הזאת.